Влияние Детензор-терапии на динамику неспецифических адаптационных реакций организма у больных с сочетанием сердечно-сосудистой патологии и остеохондроза позвоночника на этапе санаторно-курортной реабилитации
O.B. Балакирева, O.B. Tатков
Центр Естественной медицины «МЕДАРТ поликура», Москва
Военный санаторий «Чемитоквадже»
Болезни опорно-двигательного аппарата чрезвычайно распространены. В различные периоды жизни они встречаются у 20-45% населения земного шара. До 10% больных только остеохондрозом поясничного отдела позвоночника становятся инвалидами [1].
Общая распространенность заболеваний опорно-двигательного аппарата в России за 10 лет (1988-1997 гг.) выросла с 7,5 до 11,2 млн, случаев, т.е. более чем на 49% [2].
Сердечно-сосудистые заболевания также широко распространены, относятся к прогностически неблагоприятным и лидируют среди причин инвалидизации и смерти в ряде стран мира, Россия в списке этих стран занимает первое место, заметно обогнав как развитые, так и развивающиеся страны. В период 1990-1997 гг. заболеваемость ишемической болезнью сердца (ИБС) увеличилась более чем на 1 тыс. чел. на каждые 100 тыс. населения. Установлено, что около 70% населения страны живут в условиях хронического психосоциального стресса высокого и среднего уровня, что само по себе может явиться причиной первичных психогенных болевых ощущений различной локализации с дальнейшей их трансформацией в хронические, если влияние психогенной депрессии не устраняется.
Россия находится на одном из последних мест в мире по средней ожидаемой продолжительности жизни. Она составляет у мужчин 57,3 года, а у женщин – 71,1 год. 8сочетании с преждевременной смертностью населения, достигшей за последние 5 лет 14,3 на 1 тыс. чел., при рождаемости 8,9 на 1 тыс., эти проблемы уже трансформировались из сугубо медицинских в социальные, поскольку ежегодная убыль населения в 800 тыс. чел. (данные без учета эмиграции, составляющей 120-130 тыс. чел. в год) – это прямая угроза будущему нации, ее оборонному, экономическому, интеллектуальному и трудовому потенциалу [3].
За последние 30 лет структура смертности от сердечно-сосудистых заболеваний в России практически не изменилась - около 90% случаев приходится на ИБС и мозговой инсульт. Приблизительно у трети больных ИБС наблюдаются тревожные или депрессивные расстройства разной степени выраженности. При этом 90% больных ИБС имеют сопутствующую патологию позвоночника в виде остеохондроза различных его отделов [4], что, очевидно, связано с наличием в патогенезе заболеваний позвоночника и сердца общих патогенетических механизмов, реализуемых, в том числе и в виде болевого синдрома (острого и хронического) различной длительности и локализации. Существует общность и этиологических факторов патологии опорно-двигательного аппарата и сердечно-сосудистой системы, поскольку установлена четкая связь хронических мышечно-скелетных заболеваний с такими факторами риска как стресс, ожирение, снижение физической активности и курение (2].
Остеохондроз шейного и грудного отделов позвоночника в ряде случаев, наряду с характерными расстройствами, может обусловливать экстрасистолии и ощущения боли в области сердца. Эти кардиалгии клинически чаще всего входят в структуру мышечно-тонических и миофасциальных синдромов, диагностическим критерием которых является их уменьшение или исчезновение после блокад, мануальной терапии, релаксации.
Боли вертеброгенной природы и миофасциальные проявления требуют проведения мероприятий, воздействующих на вертебральные и экстравертебральные механизмы патогенеза.
Чувство боли, как известно, кардинально отличается от прочих присущих человеку чувств – слуха, зрения и т. п. Оно не имеет специального органа восприятия (подобного уху или глазу), ни специфических болевых нервов, подобных слуховому или зрительному, ни специализированного стимула: боль может возникать в результате как ожога, так и ушиба или, например, укуса. Специалисты считают боль своеобразной аварийной сигнализацией, срабатывающей в организме в критической ситуации и вызывающей в нем защитный рефлекс.
Этот рефлекс состоит в многокомпонентной оборонительной реакции, проявляющейся на всех иерархических уровнях: в изменении кровяного давления, ритма дыхания, учащении пульса, расширении зрачков, выбросе в кровь гормонов, а в целом - в изменении метаболизма.
Показано, что любая периферическая боль связана с повышением чувствительности специализированных нейронов, обозначаемых как ноцицепторы, создающих сигнал, распознаваемый как боль. Оказалось, что болевая часть «аварийного» сигнала представляет собой относительно высокочастотную (до 20 Гц) последовательность импульсов в специализированных нервных волокнах. 8 экспериментах на животных выяснено, что для подавления боли достаточно устранить («отфильтровать») эту высокочастотную составляющую.
Низкочастотная же (менее 2 Гц) часть нервного сигнала проходит через фильтр сохранной, что обеспечивает связь пораженного органа с центральной нервной системой (ЦНС), а это во многих случаях имеет принципиальное значение для лечения. Повышение чувствительности первичного ноцицептора в пораженной периферической ткани приводит к повышению активности нейронов, посылающих сигнал в спинной мозг и ЦНС, однако необходимо подчеркнуть, что в очаге воспаления может генерироваться спонтанная электрическая активность, обусловливающая стойкий болевой синдром. Таким мощным индуктором болевой чувствительности являются противоболевые компоненты: брадикинины, гистамин, нейрокинины, комплемент, оксид азота, которые обычно обнаруживаются в очаге воспаления.
Исследования показали, что при периферическом воспалении в спинномозговой жидкости повышается уровень простагландинов. Простагландины как бы включают нормальные («молчаливые») ноцицепторы в такое состояние, что они легко возбуждаются при различном воздействии. Анатомические структуры (внутренние органы) хорошо иннервированы, поэтому источником боли может быть любое анатомическое образование. Передача раздражения ноцицелторов в ЦНС, вызванная их активацией в поврежденных структурах, вызывает комплекс физиологических и психологических реакций, результатом которых является развитие мышечного спазма – защитного феномена, ограничивающего подвижность позвоночника.
Рефлекторные болевые симптомы (около 85% больных с болями в спине) обусловлены раздражением рецепторов фиброзного кольца, мышечно-суставных структур позвоночника.
Ранее считалось, что в «остром» периоде такого рода болей необходимо было добиться максимальной разгрузки позвоночника с одновременной его иммобилизацией, но в настоящее время это признано неоправданным, поскольку пациент, как правило, сам находит максимально безболезненную позу. Длительный (более 3-4 суток) постельный режим также не оправдан, так как, по концепции Вадделя, боль и длительная, необоснованная иммобилизация вызывают психологические расстройства [5-8].
Система Детензор для долговременной тракционной терапии всего позвоночного столба, разработанная в 1980 г. доктором Куртом Кинляйном (Германия) и успешно применяемая в медицине с 1982 г., исключает любой стресс для пациента и дает стойкий положительный эффект. Создаваемое длительное вытяжение позвоночного столба происходит в условиях релаксации и в оптимальных направлениях в сочетании с правильным функциональным положением позвоночника при сохранении его физиологических изгибов. Это обеспечивается конструкцией системы, имеющей эластичные ребра (рисунок а, б).
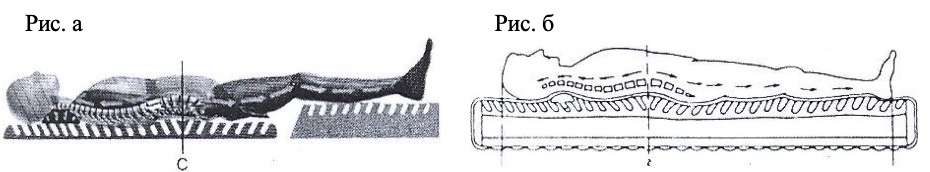
Основа лечения методом Детензор – это восстановление естественного биоритма ежедневного удлинения позвоночника путем долговременного безопасного вытяжения под действием собственной массы тела пациента.
Результаты исследований в ведущих реабилитационных клиниках России и других стран показали, что введение метода Детензор в комплекс лечебных мероприятий позволяет сократить сроки реабилитации в 1,5-2,7 раза при лечении вертеброгенного болевого синдрома различной локализации, а после оперативного вмешательства на позвоночнике (постламинэктомический синдром и др.) – в 2,5-3,5 раза.
При наличии корешкового синдрома, грыж межпозвонковых дисков, дискогенной радикулопатии в большинстве случаев достигается полный регресс болевого синдрома, клинических проявлений неврологического дефицита с восстановлением мышечной массы пораженной конечности и позы [9].
У пациентов со сколиозом I-III степени наблюдается стойкая тенденция к нормализации вертикальной оси позвоночника, протяженности и глубины лордоза и кифоза, уменьшения боковых отклонений и скручивания туловища, мышечного дисбаланса, крыловидности лопаток, перекоса таза.
В ранее проведенных исследованиях по применению лечебного тракционного мата Детензор на санаторно-курортном этапе у больных с остеохондрозом и у больных с сердечно-сосудистой патологией [10, 11], выявлено, что к концу курса лечения (18-20 ежедневных процедур по 40-45 мин) у абсолютного числа больных происходило улучшение субъективных и объективных показателей основного заболевания, сопровождавшееся нормализацией неспецифических адаптационных реакций организма и повышением уровней их реактивности, которые мы определяли по классическим критериям (табл. 1, 2) авторов теории неспецифических адаптационных реакций организма (НАРО) и основоположников активационной терапии Л.Х. Гаркави и Е.Б. Квакиной [12-15, 17].
Высокие уровни реактивности:
1. Норма по всем показателям.
2. Небольшие отклонения 1-2 (не более) показателей в пределах, указанных в графе.
Средние уровни реактивности:
1. Более двух отклонений в пределах, указанных в графе I.
2. Не более двух, указанных в графе II.
3. То и другое одновременно.
Низкие уровни реактивности:
1. Не более двух максимальных отклонений, указанных в графе II.
2. 3-4 не максимальных отклонения, указанных в этой же графе.
3. Не более двух отклонений в пределах верхней половины диапазона отклонений, указанных в графе III.
4. Более трех отклонений в пределах нижней половины диапазона отклонений, указанных в этой же графе.
5. Наличие одного отклонения, указанного в графе IV (за исключением палочкоядерных нейтрофилов).
6. Различные сочетания этих отклонений.
7. Появление в периферической крови 1-2 плазматических клеток.
Очень низкие уровни реактивности:
1. Более 3 максимальных отклонений, указанных в графе II.
2. Более 2 отклонений из верхней половины диапазона отклонений, указанных в графе III.
3. Более 4 отклонений из нижней половины диапазона отклонений, указанных в той же графе.
4. Больше одного отклонения, указанного в графе IV (за исключением палочкоядерных нейтрофилов).
5. Различные сочетания этих отклонений.
6. Появление в периферической крови незрелых клеток, которых обычно нет – от юных до миелоцитов, или более 2 плазматических клеток.
Таблица 1. Критерии адаптационных реакций по сигнальному показателю – процентному содержанию лимфоцитов в лейкоцитарной формуле
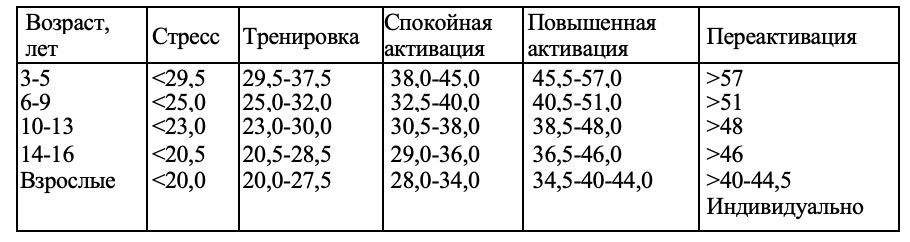
Таблица 2. Оценка уровней реактивности по выраженности признаков напряженности в лейкоцитарной формуле
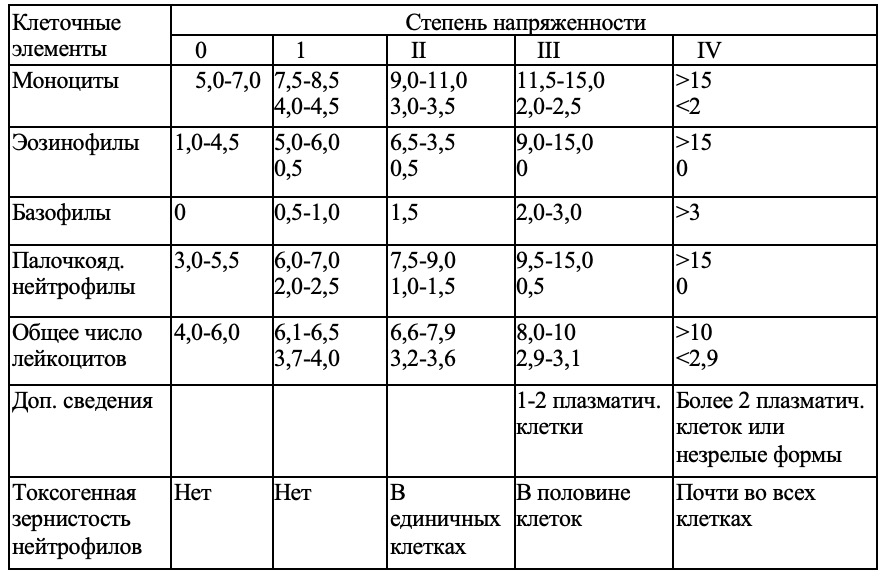
Целью настоящего исследования было изучение механизмов действия Детензор-терапии у больных с сочетанной вертебральной (остеохондроз различных отделов позвоночника) и сердечно-сосудистой (ИБС, стенокардия напряжения ФК-1, гипертоническая болезнь начальных стадий, нейроциркуляторная дистония) патологией на санаторно-курортном этапе реабилитации.
Контрольную группу отдыхающих с санаторно-курортным лечением без применения Детензор-терапии составили 56 чел. (35 мужчин и 21 женщина).
Опытную группу больных, которым в комплекс санаторно-курортного лечения была добавлена Детензор-терапия, составили 56 чел. (35 мужчин и 21 женщина).
Выяснено, что к концу лечения характер НАРО в контрольной группе мужчин существенно не менялся. Так, реакция повышенной активации (ПА) была у 11 мужчин контрольной группы до лечения, а к концу его наблюдалась у 12; реакция спокойной активации (СА) до лечения была у 8 мужчин, а к концу его – у 7; реакция тренировки (Т) до лечения была у 5 и осталась также у 5 мужчин; реакция переактивации (ПеА) в начале лечения была у 6 , а к концу лечения – у 7 мужчин; реакция стресса (С) до начала лечения наблюдалась у 5 мужчин, к концу лечения – у 4.
В опытной группе мужчин ПА в начале лечения была у 10 чел., а к концу лечения – у 22; СА в начале лечения была у 7 чел., а к концу его у 9; реакция тренировки Т в начале лечения была в 5 случаях, а к концу – в 3; ПеА в начале лечения была в 6 случаях, а после лечения – в одном; реакция стресса в начале лечения был у 7 чел., а в конце отсутствовала вовсе.
Изменения НАРО в основном произошли за счет увеличения более чем вдвое количества реакций ПА, максимально повышающих резистентность организма, снижения числа ПеА и исчезновения С (разница достоверна и определена методом альфа-углового преобразования Фишера).
У женщин контрольной группы существенных изменений характера НАРО к концу лечения также не наблюдалось: ПА была в начале лечения у 6 женщин, а к концу его – у 8; СА в начале лечения была у 4, а к концу – у 3; Т в начале лечения была у 5, к концу лечения – у 7; ПеА в начале лечения была у 4, к концу – у 2. С в начале лечения был у 2, к концу лечения – у одного.
В опытной группе женщин ПА в начале лечения была у 5 чел., к концу – у 10; СА в начале и конце лечения наблюдалась у 4 чел.; Т в начале лечения была у 5, а к концу – у 6; ПеА в начале лечения была у 4, а в конце лечения – у одного; С в начале лечения был у 3, а в конце его не было вовсе.
Таким образом, выявлено, что при добавлении к курсу лечения Детензор-терапии у женщин, как и у мужчин, резистентность значительно менялась: вдвое увеличивалось число ПА, уменьшалось количество ПеА, исчезал С (различия были на уровне тенденции 0,05 > р >0,1).
Что касается элементов напряженности реакций по другим показателям лейкоцитарной формулы, общему числу лейкоцитов и СОЗ, то в обеих контрольных группах число элементов напряженности НАРО даже несколько увеличивалось. Так, исходно, число элементов напряженности у мужчин контрольной группы по эозинофилам было 13 в начале лечения, а стало 14 в конце; по моноцитам было 6 в начале лечения, а стало 9 в конце; по общему числу лейкоцитов было 3, а стало 5 в конце лечения; по СОЗ было 9 в начале лечения, а стало 1С в конце. У женщин контрольной группы число элементов напряженности то эозинофилам было и осталось к концу лечения равным 12 случаям; по моноцитам S начале лечения было 8, а стало 10 к концу лечения; по общему числу лейкоцитов было 2, а стало 3 к концу лечения; по СОЗ было и осталось равным 5 случаям.
В опытной группе у мужчин число элементов напряженности по эозинофилам в начале лечения было 13 случаев, а стало 4 к концу лечения; по моноцитам было 8, а стало 6 к концу лечения; по общему числу лейкоцитов было 2, а после лечения не было вовсе; по СОЗ было 8 случаев в начале лечения, а стало 3 к его концу. В опытной группе у женщин число элементов напряженности по эозинофилам было 13 в начале лечения, а стало 7 к концу; по моноцитам было 7 s начале лечения, а стало 2; по общему числу лейкоцитов было а начале и осталось к концу лечения один случай; по СОЗ было в начале 5, а к концу стало 2 случая.
Как следует из представленных данных, число элементов напряженности НАРО у мужчин и женщин, которые в процессе санаторно- курортного лечения прошли курс Детензор-терапии, уменьшается к концу лечения, что свидетельствует о переходе НАРО на более высокие, физиологические уровни реактивности, значительно повышающие резистентность организма (14).
В контрольных группах существенных изменений числа элементов напряженности НАРО не произошло.
Представляющим интерес нам кажется тот факт, что у 31 из 35 мужчин опытной группы было отмечено достоверное повышение числа эритроцитов к концу лечения, выраженное в разной степени. В контроле повышение числа эритроцитов из 35 чел. было отмечено к концу лечения лишь у 4 чел. Разница статистически значима и определена по методу альфа-углового преобразования по Фишеру (8). У женщин опытной группы повышение числа эритроцитов к концу лечения отмечено в 9 случаях из 21. У женщин контрольной группы – в 3 случаях из 21.
Схематически механизм действия Детензор-терапии нам представляется следующим:
1. Воздействие на систему точек акупунктуры (ТА). ТА как специфические зоны кожи принадлежат к соматосенсорной системе, что подтверждается фактами выключения акупунктурной стимуляции путем введения местных анестетиков в глубь этих точек или в область близлежащего нервного ствола [16|.
Известно, что лечебный эффект воздействия на ТА может быть получен не только классическими методами (иглоукалывание, прижигание), но и применением охлаждения вибромассажа, вакуума, электрического тока, магнитного и электромагнитного полей, лазерного, светового и ультрафиолетового излучения, а также путем прессуры, т.е. давления, что, собственно, и происходит при сеансе Детензор-терапии, причем наибольшему давлению, согласно силе тяжести, подвергаются ТА классического Заднего Срединного Меридиана XIII (Т), который используется для специального углубленного исследования или определения отдельных функций преимущественно спинного и головного мозга (точки верхнего отдела меридиана), и вегетативной нервной системы (точки нижнего отдела меридиана). Считается, что функция этого меридиана состоит в объединении всех систем меридианов.
Стимуляция ТА вызывает повышение в спинномозговой жидкости и крови биоактивных веществ. Это приводит к сложным рефлекторным ответам, которые проявляются развитием седативных состояний, аналгезии, изменением эмоциональных реакций и психических функций. Рефлекторные ответы реализуются также в виде противовоспалительного эффекта, возвращения к нормальным показателям защитных, обменных процессов, восстановления оптимальной деятельности эндокринной, иммунной, мышечной, дыхательной, сердечно-сосудистой систем, нормализацией основных физиологических констант (пульс, АД, ЖЕЛ и пр.), – словом, к нормализации адаптации (специфической и неспецифической), одним из интегративных показателей которой являются критерии НАРО [17].
Показано, что аналгезия, возникающая при воздействии на ТА, обусловлена активацией эндогенной опиоидной системы, реализуемой выделением эндорфинов.
Опиатные рецепторы обнаружены в окончаниях чувствительных волокон, нейронах задних рогов спинного мозга, ретикулярных ядрах ствола мозга, таламусе, лимбической системе. В последние годы идентифицированы нейропептиды (эндорфины и энкефалины), специфически воздействующие на эти рецепторы и дающие, в связи с этим морфиноподобный эффект.
Действие эндорфинов и энкефалинов блокирует выделение субстанции Р из окончаний чувствительных волокон и уменьшает болевые ощущения.
Как установлено в последнее время, эндорфины в нашем организме оказывают нормализующее воздействие на работу многих систем и органов, иммунитет, ускоряют заживление [7]. Развитие физиологических антистрессорных реакций приводит к активации эндогенной опиоидной системы [17].
2. Антидепрессивный эффект Детензор-терапии. Хроническая боль (длительность более 6 мес) – это боль, которая перестала зависеть от основного заболевания или повреждающего фактора и развивается по своим законам. Формирование хронической боли зависит в большей степени от комплекса психологических факторов, нежели от характера и интенсивности периферического воздействия. Особую роль в возникновении хронической боли играет депрессия, и этот синдром обозначают как депрессия-боль. Клинически хроническая боль является излюбленной маской скрытой депрессии. Депрессию в настоящее время предлагают рассматривать как новый фактор риска ИБО [18]. Показано, что депрессия характерна для хронического стресса [17].
Выяснено, что недостаточность серотонинергических механизмов является общей основой для формирования хронических болевых и депрессивных проявлений. Снижение уровня серотонина приводит к понижению болевых порогов и усилению боли.
Клинические наблюдения показали, что в большинстве случаев уже при проведении первой процедуры Детензор-терапии в течение 10-15 мин происходило значительное уменьшение или полное исчезновение болевого синдрома. После отмеченного уменьшения или снятия болей пациенты отмечали сонливость, а затем, по окончании процедуры, - бодрость и повышение общего тонуса, которые нарастали по мере проведения курса Детензор-терапии, к концу его становились устойчивыми и сохранялись до полугода (данные почтового анкетирования).
Известно, что при развитии любой НАРО различают две стадии: первую, быструю, преимущественно нервно-рефлекторную (гуморальный компонент, конечно, имеется) и вторую, медленную, преимущественно гуморальную. Уже через 10-15 мин после начала развития реакции в периферической крови регистрируются изменения, характерные для развивающейся НАРО. Затем начинают развиваться волнообразные колебания, регистрируемые в периферической крови как изменения количества форменных элементов (сигнальных показателей) крови (примерно через 6 ч после воздействия), которые по достижении 24 ч после начала воздействия становятся стойкими и отражают изменения (классические признаки), свойственные развившейся НАРО. С волнообразностью изменений «возбуждение-торможение», как нам представляется, связана отмечаемая пациентами сонливость после уменьшения (снятия) болевого очага возбуждения.
Многие больные отмечали, что устранение болей снимало психологический дискомфорт, значительно повышало общий тонус и общую работоспособность (профессиональную мотивацию). Помимо устранения болевых ощущений, нормализовался сон и исчезала раздражительность, возрастала переносимость психоэмоциональных и физических нагрузок, нормализовались некоторые показатели деятельности сердечно-сосудистой системы (пульс, АД), исчезали метеопатические реакции. В контрольной группе эти изменения также имели место, но были менее выражены, наступали позднее и не сохранялись более 1-2 мес. после окончания санаторно-курортного лечения.
Эти изменения психофизического состояния характерны для физиологических антистрессорных реакций, особенно реакции ПА [17].
3. Прямое воздействие Детензор-терапии на позвоночник. Под воздействием Детензор-терапии происходит мягкая тракция позвоночного столба, что приводит к разгрузке позвоночника как физической конструкции, а с другой стороны, начинается улучшение кровоснабжения страдающего сегмента позвоночника, протекающее совместно с улучшением функционирования головного мозга, о чем свидетельствует восстановление фазнотонического нистагма [19], существенно зависящего от функционального состояния различных структур мозга (стволовой части, мозжечка) и являющегося результатом интегративного взаимодействия отделов двигательной и вестибулярной систем организма, На эти изменения организм, являющийся сложной саморегулирующейся на различных уровнях системой, реагирует началом (минуты), а затем и завершением (сутки) развития какой-либо НАРО [14].
Смысл вытяжения сводится к растяжению спазмированных паравертебральных мышц, поскольку «растянуть» позвонки с помощью груза невозможно даже теоретически [19].
Тракционная терапия позволяет уменьшить функциональные нарушения в позвоночнике, связанные с ограничением его подвижности в двигательном сегменте или формированием его обратимого блокирования. Наиболее перспективной на курорте сейчас считается комплексная механотерапия - комбинация естественного последовательного нагружения позвоночника под воздействием собственного веса (основной физический смысл Детензор-терапии), периодического массажа мышц, применения природных и преформированных курортных факторов.
4. Воздействие Детензор-терапии на неспецифические адаптационные механизмы. Как показало выполненное исследование, к концу санаторно-курортного лечения у пациентов опытной группы чаще всего наблюдалось развитие реакции повышенной активации, которая наиболее значительно повышает неспецифическую резистентность организма [12, 13]. Далее, в порядке убывания, отмечалось развитие реакций спокойной активации и тренировки.
В мозгу при развитии реакции повышенной активации преобладает физиологическое возбуждение. При развитии реакции спокойной активации секреция глюкокортикоидов находится в пределах нижней половины зоны нормы, а при развитии реакции повышенной активации – в пределах верхней половины зоны нормы, что свидетельствует о наличии противовоспалительного эффекта. При этих реакциях отмечается преобладание анаболических процессов в организме и оптимальное функционирование систем энергетического обмена [14, 15, 17]. Это представляется нам одним из главных эффектов Детензор-терапии, поскольку происходит разрыв «порочного круга» патологических реакций, превалирующих при стрессовых ситуациях, характеризующихся формированием катаболической ситуации в обмене веществ, что, собственно, и приводит к патологическим изменениям как в сердечно-сосудистой системе, так и в опорно-двигательном аппарате. При развитии реакции тренировки активность желез внутренней секреции находится в пределах нижней половины зоны нормы, что и обусловливает противовоспалительный эффект, наблюдаемый при этой реакции. Секреция глюкокортикоидов, называемых «гормонами нагрузки», возрастает при снижении уровней реактивности НАРО и, наоборот, уменьшается при возрастании уровней реактивности НАРО. Увеличение секреции глюкокортикоидов на низких уровнях реактивности привносит элементы напряженности, свойственные стрессу.
Активность же других эндокринных желез – щитовидной, половой, а также гормонов коры надпочечников, не относящихся к глюкокортикоидам (за исключением АКГГ) – наибольшая (в пределах физиологической нормы) при реакциях повышенной активации, затем спокойной активации затем тренировки. Со снижением уровней реактивности - увеличением абсолютной величины управляющего фактора – секреция указанных гормонов, напротив, снижается.
Изменения в системе иммунитета наиболее благоприятны (физиологически оптимальны) при реакциях повышенной и спокойной активации, при которых, помимо указанных характеристик, наблюдается высокая активность иммунной системы, особенно клеточной ее составляющей – Т-лимфоцитов-киллеров.
Меньшая активность иммунитета (но в пределах нижней половины зоны нормы) характерна для реакции тренировки. При снижении уровней реактивности активность иммунной системы также снижается, но в пределах значений, свойственных развившейся реакции.
Изменения организма при различных НАРО носят универсальный характер, хотя специфический фактор, вызвавший ту или иную НАРО, диктует свои особенности. Полученные данные позволяют говорить о потенцирующем воздействии Детензор-терапии на различные иерархические уровни системы адаптации организма. Сочетание механизма общего и местного воздействия при лечении сердечно-сосудистых заболеваний и остеохондроза, имеющих местный очаг патологии, по нашему мнению, наиболее эффективно, особенно при целенаправленном развитии в организме реакций повышенной и спокойной активации. НАРО вызывают изменения на различных иерархических уровнях организма, вплоть до субклеточных.
В случаях, ада местный патологический очаг отсутствует, реакции на разных иерархических уровнях являются лишь составной частью общей НАРО. По показателям данного иерархического уровня при ПА отмечается наиболее высокий уровень активности – на верхней границе нормы; при СА – о пределах верхней половины зоны нормы; при Т – в пределах нижней половины зоны нормы; при ПеА – выше нормы, а при С – ниже нормы. При наличии патологического очага почти всегда наблюдается несоответствие общей и местной реакции. В этих случаях особенно важно сочетание общего и местного действия на патологический очаг.
Мы считаем, что дополнительная импульсация с места патологического очага и ответная - в патологический очаг способствуют усилению регулируемости местного процесса с помощью всех имеющихся в организме регуляторных механизмов, а затем и подключению исполнительных звеньев, реализующих процессы нормализации. При этом в процессе нормализации участвуют различные местные неспецифические реакции, - от стресса, вызывающего гибель патологически измененных структур и тканей, до активации, приводящей к нормализации деятельности тканевых структур, местного иммунитета, активности соединительной ткани и трофики очага патологии [17].
Литература
1. Насонов Е.Л. Болевой синдром при патологии опорно-двигательного аппарата Врач. 2002. № 4. С. 15-19.
2. Насонова В. А., Халтаев Н.Г. Международное десятилетие болезней костей и суставов – многодисциплинарная акция //Тер. архив. 2001. № 5. С. 5-7.
3. Татков О. В, Липидный спектр крови и адаптационные реакции у больных с сердечно-сосудистой патологией на санаторно-курортном этапе реабилитации: Автореф. дис. ... канд. мед. наук. – Ростов на/Д, 2000. С. 22.
4. Арутюнян Р.Ю., Князева Т.А. Эффективность мануальной терапии при реабилитации больных с ишемической болезнью сердца // Вопросы курортологии, физиотерапии и лечебной физической культуры. 2001. № 2. С. 3-6.
5. Вейн А.М., Данилова АБ. Кардиалгии и абдоминалгии // Русский медицинский журнал. 1999. № 9. С. 428-433.
6. Насонова В.А. Значение циклооксигеназы-2 в развитии боли. // Тер. архив. 2001. № 5. С. 56-57
7. Филатова Е.Г., Вейн А.М. Фармакология боли //Рус. мед. журн. 1999. №9. С. 410-418.
8. Черненко О.А. Лечение болевых скелетно-мышечных поясничных синдромов // Рус. мед. журн. 2000. № 10. С. 408-410.
9. Результаты внедрения терапевтической системы Детензор в комплекс реабилитационных мероприятий больных неврологического профиля / В.И. Шмырев, А.И. Романов, К.Л. Кинляйн, Т.С. Ракова, О.В. Балакирева / Клин, вести 1996 №4. С. 59-61.
10. Применение лечебного мата Детензор в реабилитации летного состава / Ю.Б. Моисеев, Н.В. Ромасюк, А.В. Соломка, О.В. Тагков. // Воен.-мед. журн. 1999. № 10. С. 64.
11. Татков О.В., Ромасюк Н.В. Эффективность применения лечебного мата Детензор в санаторно-курортной практике реабилитации больных с сердечно-сосудистой патологией // Достижения и перспективы медицинской реабилитации. Сочи, 1999. С. 160-161.
12. Гаркави Л.Х. Об общей неспецифической адаптационной «реакции активации», способствующей борьбе организма с опухолью // Вопросы клинической онкологии и нейроэндокринных нарушений при злокачественных новообразованиях. Ростов на/Д, 1968. С. 341-348.
13. Гаркави Л.Х. Реакция активации – общая неспецифическая адаптационная реакция на раздражители «средней силы» // Адаптационные реакции и резистентность организма. Ростов на/Д, 1990. С. 36-63.
14. Гаркави Л.Х., Квакина Е.Б. О принципе периодичности в развитии адаптационных реакций и ареактивности // Адаптационные реакции и резистентность организма Ростов на/Д, 1990. С. 64-100.
15. Гаркави Л.Х., Квакина Е.Б. О критерии оценки неспецифической резистентности организма при действии различных биологически активных факторов с позиции теории адаптационных реакций // М.: М.-волны в биологии и медицине. 1995. № 6. С. 11-21.
16. Нетрадиционные методы диагностики и терапии / И.З. Самосюк, В.П. Лысенюк, А.К. Лиманский, А.Н. Повжитков, Р.Р. Бойчук, В.Я. Антонченко. Киев: Здоровья, 1994. С. 240.
17. Гаркави Л.Х., Квакина Е.Б., Кузьменко Т.С. Антистрессорные реакции и активационная терапия. М.: Имедис, 1998. С. 656.
18. Погосова Г.В. Депрессия – новый фактор риска ишемической болезни сердца и предиктор коронарной смерти // Кардиология. 2002. № 4. С. 86-90.
19. Изучение влияния Детензор-терапии на восстановление фазнотонического нистагма / Р.Р. Каспранский, О.В. Тагков, Б.Б. Кедров, О.В. Балакирева // Современные технологии восстановительной медицины. Сочи, 2002. С. 217-218.
20. Качков И.А., Филимонов Б.Л., Кедров А.В. Боль в нижней части спины//Рус. мед. журн. 1997. № 15. С. 997-1012.
21. Гублер Е.В. Вычислительные методы анализа и распознавания патологических процессов. М.: Медицина, 1978. С. 84-96.
